De afgelopen tientallen jaren hebben we veel meer inzicht gekregen in de mechanismen van bacteriën om de werking van antibiotica te omzeilen. Tot op het atoom nauwkeurig weten we hoe en waar de antibiotica aangrijpen; en welk antwoord de bacterie ontwikkelt om dat aangrijpingspunt onbruikbaar of ontoegankelijk te maken. Toch heeft al dit inzicht niet of nauwelijks geleid tot nieuwe antibiotica; laat staan betere. Merkwaardig. Is er wat mis met onze aanpak of denkwijze? Onze manier van werken is nogal reductionistisch. We willen één ziekmakende bacterie treffen in één specifieke eigenschap. Dat doen we met één antibioticum dat precies die eigenschap frustreert. Als resistentie optreedt bestrijden we dat weer met één specifieke aanpak. Misschien moeten we wat meer holistisch te werk gaan; meer pijlen tegelijk afschieten. Een mutatie komt ook nooit alleen. Of misschien moeten we meer combinatietherapieën gaan ontwikkelen zoals in Augmentin.
Project ‘100 jaar antibiotica’
Aflevering 48. De zoektocht naar nieuwe antibiotica, 2000-2020
Aflevering 49. Verder met de oude wapens?
Aflevering 50. Resistentie nader bekeken
Aflevering 51. Nieuwe antibiotica, zo gaat het ook niet. Het relaas van lefamuline
Aflevering 52. Zicht op nieuwe middelen??
Resistentie als natuur-verschijnsel
Micro-organismen als ziekteverwekkende bacteriën staan continu bloot aan een vijandige omgeving. Ze worden belaagd door soortgenoten, virussen, fagen en soms ook door medicijnen als antibiotica. In hun omgeving is voortdurend verandering gaande, en zij evolueren mee. Misschien zijn daardoor veel natuurlijke antibiotica zo enorm ingewikkeld van structuur en zo divers van samenstelling. De continue omgevingsdruk heeft de micro-organismen ook ‘geleerd’ om verdedigingsmechanismen op alle mogelijke manieren aan elkaar door te geven. Inclusief het uitwisselen van genetische informatie en ‘geheimen’ om belagers tegemoet te treden. Genetische manipulatie is een alledaags verschijnsel in de wereld van micro-organismen. Elementen van resistentie zijn gevonden in 30.000 jaar oud DNA van bacteriën uit de permafrost. Elke willekeurige bacterie uit de grond laat kenmerken van resistentie zien; ook al zijn ze de betreffende antibiotica nooit tegengekomen. Het uitbundig humaan en veterinair gebruik van niet veel meer dan een halve eeuw heeft de bacteriën alleen maar een beetje slimmer gemaakt.
Hoe groot is het probleem?
De literatuur en het nieuws overladen ons met de risico’s van resistentie. De getallen die ze ons voorschotelen zijn vaak indrukwekkend. Maar vaak beschikken we niet over vergelijkingsmateriaal waarmee we de informatie op waarde kunnen schatten. Een voorbeeld. De kans om aan een bacteriële infectie te overlijden is tientallen malen kleiner dan in de tijd van onze grootouders. Maar wij redeneren vanuit een nagenoeg nul-risico en dan slaat angst of zorg snel toe. Ter oriëntatie enkele grove cijfers over de belangrijkste doodsoorzaken van de afgelopen tien jaar (wereldwijd).
– Wereldwijd is het aantal sterfgevallen ca. 160.000 per dag
– Daarvan is ca. 75% te wijten aan niet-besmettelijke ziektes; daarvan weer 2/3 aan kanker en aandoeningen van hart en bloedvaten (80.000 per dag)
– En ca. 15% van de sterfgevallen is te wijten aan besmettelijke ziektes; daarvan vormen luchtweginfecties met bijna de helft de grootste groep. TBC is met 3.000 doden per dag de meest voorkomende enkelvoudige infectie.
De belangrijkste gevaarlijke bacteriële infecties zijn: miltvuur, tetanus, leptospirose (o.a. ziekte van Weil), tbc, longontsteking, cholera, botulisme, pseudomonas, MRSA infecties, hersenvliesontsteking, gonorroe, pest en syfilis.
Uiteraard treffen we resistente organismen vooral aan op de plekken waar antibiotica het meest worden gebruikt: verpleeghuizen, ziekenhuizen en de (intensieve) veehouderij. De kans om de vervelende ziekenhuisbacterie, C.difficile, op te lopen is meer dan 50% bij een verblijf van 4 weken in het hospitaal. Gelukkig is het gebruik van antibiotica in de Nederlandse veehouderij sinds 2015 met meer dan de helft afgenomen.
Deskundigen hebben overzichten gemaakt van resistentie: onder welke bacteriestammen komt resistentie voor tegen welke antibiotica. Zulke lijsten zijn lang. In feite zijn er geen middelen waarmee we alle gevaarlijke bacteriën kunnen uitschakelen; maar dat is ook nooit het geval geweest.
Wat zijn de strategieën van de verdedigers
In de voorgaande afleveringen hebben we laten zien dat antibiotica de bacterie op verschillende manieren kunnen aanpakken. Bij de werking onderscheiden we vijf groepen. Twee daarvan grijpen aan op de celwand. De eerste door de opbouw van de celwand te verstoren of onmogelijk te maken; zodat de bacterie als het ware wordt lek geprikt. Helaas hebben niet alle ziekmakers een celwand. De tweede groep verandert de eigenschappen van de celwand zodat het middel alsnog naar binnen kan glippen. Ze kunnen een vettige celwand hydrofiel maken; of ze kunnen de polariteit (ladingsverschillen) op de wand verschuiven. Een drietal groepen antibiotica doet zijn werk binnen in de bacterie. Een grote groep verstoort de opbouw of de werking van de genetische code. Een andere groep middelen belemmert de aanmaak van belangrijke eiwitten. En een laatste groep frustreert allerhande processen in de cel, zoals het transport of de aanmaak van essentiele moleculen (denk aan de belemmering van de productie van foliumzuur door de sulfa’s).
Tegenacties
Veel verdedigings-mechanismen van de bacterie berusten op natuurlijke, inherent aanwezige eigenschappen. Een vettige, hydrofobe celwand zal geladen of waterminnende middelen niet eenvoudig doorlaten. Ook hebben de meeste bacteriën een mechanisme, een pomp, waarmee ze onbekende moleculen zo snel mogelijk de cel weer uit kunnen werken. We kennen wel 5 verschillende types van zulke ‘pompen’. Soms worden deze pas geinstalleerd of geactiveerd als een nieuw vreemd molecule (een nieuw antibioticum) in de buurt komt. Alle levende cellen hebben overigens een scala aan transportsystemen. Logisch, want al die DNA onderdelen, eiwitten, vetten, suikers en wat niet al moeten niet alleen worden gemaakt maar ook op de juiste plaats worden gebracht. Allemaal óók mechanismen waarmee de cel een ongewenst product kan wegwerken; of andersom: waarmee een geneesmiddel kan worden binnengesmokkeld.
Verder zal elke bacterie in actie komen tegen alle middelen die zijn bestaan bedreigen. Dan is het arsenaal aan mogelijkheden groot. Veranderingen in het metabolisme (de processen in de cel). De genetische machinerie (mutaties). En vooral het overnemen van genetische verbeteringen van andere soortgenoten. Soms nemen bacteriën zelfs resistentie over van andere micro-organismen als virussen of fagen. We weten niet in hoeverre zulke mutaties willekeurig zijn; maar mutanten die een antibioticum effectief aanpakken zullen de beste kansen op overleving hebben. Mutaties kunnen wel gepaard gaan met verzwakking van de bacterie op andere punten. Al deze middelen kunnen worden ingezet om de belager alsnog de cel uit te werken; of om de belager onschadelijk te maken; danwel om het doel van de belager te veranderen of onbereikbaar te maken. Belangrijk voorbeeld: de al besproken bèta-lactamase enzymen die vroeg of laat de werking van elk penicilline- of cefalosporinemolecuul belemmeren.
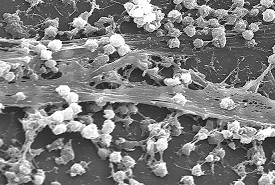
Samen sterk
Een bijzonder verdedigingsmechanisme van de bacterie is de vorming van een biofilm; een plakkerig geheel van vele samenklonterende cellen van dezelfde of verschillende bacteriesoorten. Ook wij maken zulke biofilms in onze (gezonde) maag-darm flora; daarmee kunnen we een aanval op ons immuunsysteem overleven. De bacteriën zijn in de film omhuld door een laag suikers met daarin ook eiwitten en DNA-materiaal. Daardoor wordt het binnendringen van vreemde moleculen (antibiotica) extra moeilijk. Bovendien groeien de bacteriën in de filmkolonie langzaam; ook daardoor zijn ze minder gevoelig voor middelen die groei of celdeling belemmeren. Het meest belangrijk is evenwel dat de bacteriën in de film extra kansen krijgen om genetische eigenschapen uit te wisselen. Resistentie bijvoorbeeld.

Een eeuwige strijd
In de volksmond is de MRSA bacterie bekend als erg gevaarlijk en resistent tegen heel veel middelen. Zijn track record is inderdaad indrukwekkend. Zie de tabel: de bacterie gebruikt alles uit zijn arsenaal meer of minder effectief tegen nagenoeg alle middelen die we kennen.
Geraadpleegde bronnen:
Wikipedia: alle genoemde eigennamen en producten
Lijst van door de FDA goedgekeurde middelen 1999-2021
Antibiotics and bacterial resistance in the 21st century, R.J. Fair en Y. Tor, Perspectives in Medicinal Chemistry 6, 25-64 (2014)
An overview of the antimicrobial resistance mechanisms of bacteria, Wanda C Reygaert, AIMS Microbiol. 2018; 4(3): 482–501
Antibiotic Resistance Fact Sheets, WHO.
