In de wereld van de micro-organismen zijn er geen leiders. Iedereen heeft vrienden en vijanden. Sommige zijn echt levende wezens, anderen staan op het snijvlak van leven en niet-leven. Of ze zijn alleen maar werkzaam in een wisselwerking. Micro-organismen vormen een zeer bonte samenleving, bijna allemaal eencelligen of kleiner dan dat. Zo ook de bacteriofagen of kortweg fagen; virussen die een bacterie infecteren. Meestal doen deze dat door hun genetisch materiaal in de bacterie in te spuiten. De bacterie wordt daardoor aangezet tot het maken van nieuwe fagen. Uiteindelijk barst de bacterie open, waarbij de nieuwe fagen worden uitgestoten – een zeer snel vermenigvuldigingsmechanisme. Maar al te zeer bekend uit de coronapandemie.
Project ‘100 jaar antibiotica’
Aflevering 54. Als chemie en biotech samen optrekken
Aflevering 55. Antibiotica en onze maag-darmflora
Aflevering 56. Bacteriofagen: bijna vergeten, maar….
Aflevering 57. Faagtherapie, een veelbelovend alternatief voor antibiotica?
Aflevering 58. Natuurlijke geneesmiddelen
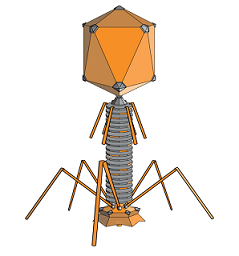
Bacteriofagen: voor- en nadelen
Fagen zijn zeer specifiek: de meeste kunnen alleen één bacteriesoort aantasten. Ten opzichte van chemische antibiotica, die vele bacteriesoorten tegelijk aantasten, is dat een groot nadeel. Want voor elke infectie moet de arts een faag vinden die precies de betreffende bacterie aantast. Tegelijkertijd is dit een groot voordeel. Want andere bacteriën dan de schadelijke bacterie worden niet aangevallen – terwijl een antibioticakuur bijvoorbeeld ook een groot deel van de nuttige bevolking van de darmen vernietigt.
De voorgeschiedenis
Fagen worden ontdekt aan het begin van de vorige eeuw. In 1915 door de Britse bacterioloog Frederick Twort. En onafhankelijk van hem in 1917 door de Frans-Canadese microbioloog Félix d’Hérelle. Twort kan niet verder werken aan bacteriofagen, door de Eerste Wereldoorlog en gebrek aan geld. Maar juist deze oorlog geeft het werk van d’Hérelle (1873-1949) een grote impuls. Hij is een avontuurlijke ondernemer. In Noord- en Midden-Amerika houdt hij zich bezig met het bestrijden van plantenziektes en het stoken van alcoholica. In 1911 gaat hij met zijn gezin naar Parijs. Daar raakt hij onder meer betrokken bij het Pasteur Instituut in onderzoek naar de bestrijding van sprinkhanen. Zijn eerste succes is een microbieel preparaat uit het spijsverteringskanaal van dezelfde sprinkhanen. Vervolgens isoleert hij uit kippenmest een preparaat, een faag zoals naderhand blijkt, tegen tyfus bij kippen.
De werkwijze berust erop dat een bacteriekweek op goede ondergrond (bijv. kippenmest) op een gegeven ogenblik helder en doorzichtig wordt; een teken dat de bacterie is besmet met fagen en bezig is daaraan ten onder te gaan. Filtreren levert het therapeutische preparaat. Zijn eerste succes bij mensen is de behandeling van dysenterie met een dergelijk preparaat uit een gefilterde oplossing van uitwerpselen van dysenterielijders. Een groot probleem in de loopgraven van WO I. Hij stelt de juiste diagnose: dat hij te maken heeft met een virus dat parasiteert op de bacteriën. De naam bacteriofaag stamt ook van hem, deze betekent ‘organisme dat bacteriën eet’.
Wisselende resultaten
Félix d’Hérelle is een avontuurlijke man zonder academische opleiding, die overal aan de slag gaat waar men zijn hulp denkt te kunnen gebruiken; van Argentinië tot India en van Alexandrië tot Parijs. De ziekten die hij probeert te bestrijden lopen uiteen van dysenterie tot cholera en de pest. Rond 1924 is er een ware hype over de mogelijkheden van faagtherapie. Maar er blijven twijfels bestaan over zijn methode. De resultaten wisselen sterk, misschien door onzuivere stoffen, misschien door lage concentraties van de fagen. Fagen isoleren of karakteriseren lukt niet. Bestaan ze wel? Is het filtraat niet simpel een opgelost enzym? En kijk naar Fleming, die zat in diezelfde jaren te worstelen met de identiteit van zijn penicilline. Hierdoor komt er ook een eind aan de beginnende belangstelling van het Amerikaanse farmaceutische bedrijf Eli Lilly. Pas in 1939 toont onderzoek met de elektronenmicroscoop het bestaan van bacteriofagen werkelijk aan. Bovendien blijkt d’Hérelle met Jan en alleman ruzie te maken. Hoewel: In 1924 ontvangt d’Hérelle een eredoctoraat van de universiteit van Leiden alsook de Van Leeuwenhoek medaille.

Georgië
Maar op één plaats heeft hij een blijvende invloed, in Tblisi in Georgië. Daar is George Eliava hoofd van het centraal bacteriologisch laboratorium. Eliava en d’Hérelle hebben elkaar leren kennen op het Pasteur Instituut in Parijs. Eliava wordt enthousiast over de mogelijkheden van bacteriofagen in de medische praktijk en wijdt zijn werk in Georgië daaraan. In 1923 bestudeert hij de cholerabacterie in monsters uit de rivier de Mtkvari. Na drie dagen blijkt de bacterie verdwenen en Eliava legt de link met de bacteriofagen. Binnen een paar jaar hebben de onderzoekers meer dan twaalf fagen gevonden die vele bacteriële infecties kunnen bestrijden.
Maar Eliava valt in ongenade bij Stalin. Misschien doordat hij een intellectueel is; maar misschien doordat hij het hof maakt aan de vrouw die ook wordt begeerd door Lavrenti Beria, hoofd van Stalins geheime politie. Hij wordt tot vijand van het volk verklaard en geëxecuteerd in 1937. D’Hérelle kan dan al niet meer Georgië in; na een bezoek aan Parijs in 1935 wordt hij tot ‘ongewenste buitenlander’ verklaard. Hij overlijdt in 1949. Een vergeten man, zelfs al is hij tien keer voorgedragen voor de Nobelprijs.
Bijna vergeten
Het werk van Eliava in Georgië wordt voortgezet in een naar hem genoemd instituut. Bacteriofagen worden er zelfs onderdeel van de reguliere geneeskunde. In de Tweede Wereldoorlog worden ze vaak gebruikt bij behandeling van gewonde Sovjetsoldaten, onder meer bij gangreen. Daarna verhindert de oprichting van het IJzeren Gordijn de uitwisseling van kennis tussen Oost en West. Sovjet-medici publiceren wel over bacteriofagen, maar alleen in het Russisch. Uiteindelijk wordt ook in de Sovjetunie het werk aan bacteriofagen verdrongen door de opkomst van antibiotica. Tegen het midden van de jaren 1970 ligt het werk aan het Eliava Instituut praktisch stil. De onderzoekers bewaren faagmonsters in koelkasten thuis om te voorkomen dat ze verloren gaan. In 1993 wordt het instituut echt gesloten. Hier en daar past men de faagtherapie dan nog toe, in Georgië en in mindere mate ook in Polen.
Maar in de 21e eeuw dringt de ernst van antibiotica-resistentie door tot de wereld. Het leidt tot nieuwe belangstelling voor bacteriofagen.
Geraadpleegde bronnen:
Wikipedia: alle genoemde eigennamen en producten
